Gesetz von Dalton
Das Gesetz von Dalton beschreibt, wie sich die Partialdrücke (Teildrücke) der verschiedenen Gase eines Gasgemisches aus den Gasanteilen und dem Gesamtdruck des Gemisches ergeben.
Der Partialdruck eines Gases in einem Gasgemisch ist dabei der Druck, der sich ergeben würde, wenn in dem entsprechend gleichen Volumen nur dieses eine Gas vorhanden wäre. In Summe ergeben alle Partialdrücke der Anteile eines Gasgemisches dessen Gesamtdruck.
Wissen für fortgeschrittene Taucher (ED**)
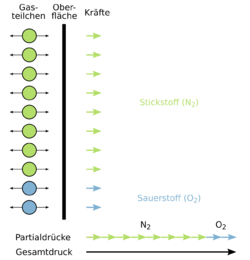
Der Gasdruck entsteht durch die Kollision der Gasteilchen mit den Oberflächen eines Behältnisses. Da z. B. Luft aus mehreren verschiedenen Gasarten besteht, wird ein Teil des Gesamtdrucks durch das Auftreffen der Stickstoffmoleküle und ein Teil durch das der Sauerstoffmoleküle erzeugt.
Die verschiedenen Teil- bzw. Partialdrücke errechnen sich aus dem Gesamtdruck multipliziert mit dem Gasanteil. Im Fall von Luft bei einem Druck von 1 bar ergibt sich ein Sauerstoffpartialdruck von 0,21 bar, ein Stickstoffpartialdruck von 0,78 bar und 0,01 bar entfallen auf die restlichen Luftbestandteile. In Summe ergeben alle Partialdrücke den Gesamtdruck des Gasgemisches.
| Wasser- tiefe |
Umgebungs- druck |
Sauerstoff- partialdruck |
Stickstoff- partialdruck |
|---|---|---|---|
| 0 m | 1 bar | 0,21 bar | 0,78 bar |
| 10 m | 2 bar | 0,42 bar | 1,56 bar |
| 20 m | 3 bar | 0,63 bar | 2,34 bar |
| 30 m | 4 bar | 0,84 bar | 3,12 bar |
| 40 m | 5 bar | 1,05 bar | 3,90 bar |
Entgegen der landläufigen Meinung hängt die Wirkungsweise oder Schädlichkeit eines Gases hängt nicht von seinem prozentualen Anteil, sondern von seinem Partialdruck ab:
- Fast alle Bezwinger des Mount Everest benötigen auf dem obersten Abschnitt des Aufstieges Zusatzsauerstoff, obwohl die Luft dort oben genauso wie im Tal 21% Sauerstoff enthält. Der Umgebungsdruck am Gipfel liegt aber nur bei etwa 0,33 bar. Daraus berechnet sich ein Sauerstoffpartialdruck von nur etwa 0,07 bar, was für einen Menschen ohne Höhentraining viel zu wenig zum Überleben wäre. In der Regel ist ein Sauerstoffpartialdruck von mindestens 0,15 bar notwendig.
- Sauerstoff wirkt allerdings auch bei zu hohem Partialdruck toxisch. Man sollte einen O2-Partialdruck von 1,4 bar nicht überschreiten. Gerade bei Verwendung von Nitrox kann diese Grenze, je nach Sauerstoffanteil, schon bei 20 m bis 30 m erreicht werden.
- Der CO2-Partialdruck in der Ausatemluft wird durch den CO2-Spiegel im Blut definiert. Bei normaler Aktivität und Atmung wird dieser über das Atemzentrum auf einem annähernd konstanten Wert gehalten. In diesem Fall beträgt der CO2-Partialdruck in der Ausatemluft etwa 0,04 bar. An der Wasseroberfläche bei einem Umgebungsdruck von 1 bar entspricht dies einem Anteil von etwa 4% Kohlendioxid in der Ausatemluft.
Expertenwissen (DM***)
Der Partialdruck eines Gases [math]p_{\text{gas}}[/math] berechnet sich aus dem Anteil des Gases [math]f_{\text{gas}}[/math] und dem Gesamtdruck des Gasgemisches [math]p[/math] über:
- [math]p_{\text{gas}} = f_{\text{gas}}\ \cdot\ p[/math]
Der Partialdruck eines Gases hängt somit nicht nur von der Tauchtiefe, d. h. dem Umgebungsdruck unter dem es geatmet wird, ab, sondern auch von der Zusammensetzung des Atemgases.
Um das Risiko einer ZNS-Sauerstoffvergiftung zu minimieren, sollte ein Sauerstoffpartialdruck von 1,4 bar nicht überschritten werden. Für Luft mit einem Sauerstoffanteil von 21%, d. h. [math]f_{\text{gas}} = 0,21[/math] , beträgt der maximale Umgebungsdruck unter dem Luft geatmet werden darf 6,6 bar. Das entspricht einer Tiefe von 56 m und liegt somit jenseits der üblichen Sporttauchgrenze von 40 m.
Wird ein typisches Nitroxgemisch mit 32% Sauerstoffanteil verwendet, beträgt der maximal zulässige Umgebungsdruck 4,375 bar. Die maximale Tiefe, die nicht überschritten werden darf (MOD), liegt somit bereits bei 33 m. Der Stickstoffpartialdruck, der für die Stickstoffsättigung und somit die Dekompressionsberechnung relevant ist, reduziert sich im Vergleich zu Luft bei gleicher Tiefe allerdings.
Spezialwissen (Nitrox*)
Die Partialdrücke [math]p_{\text{gas}}[/math] der Anteile eines Gasgemisches errechnen sich aus dem Gesamtdruck des Gasgemisches [math]p[/math] multipliziert mit dem Gasanteil [math]f_{\text{gas}}[/math].
- [math]p_{\text{gas}} = f_{\text{gas}}\ \cdot\ p[/math]
Die Summe dieser Partialdrücke ergibt den Gesamtdruck des Gasgemisches.
Bei einem Nitrox-Gasgemisch wird der Sauerstoffanteil im Vergleich zu Luft erhöht, wodurch sich der Stickstoffanteil verringert. Bei gleichem Umgebungsdruck, d. h. gleicher Tauchtiefe, vergrößert sich bei steigendem O2-Anteil somit der Sauerstoffpartialdruck. Dies verringert die maximale Einsatztiefe des Atemgases.
Gleichzeitig verkleinert sich allerdings der Stickstoffpartialdruck, der für die Stickstoffsättigung relevant ist. Hieraus resultieren längere Nullzeiten.